Луиджи Риккарди 1 , Роза Маццео 2,*© , Анджело РаffЭль Маркотриджано 1 , Гульельмо Райнальди 3 , Паоло Иовьено 4 , Вито Зонно 1 , Стефано Паван 1 © и Кончетта Лотти 2,*
- 1 Департамент почвенных, растительных и пищевых наук, Отделение генетики и селекции растений Университета Бари, Via Amendola 165/A, 70125 Бари, Италия; luigi.ricciardi@uniba.it (ЛР);angelo.marcotrigiano@uniba.it (РУКА); vito.zonno@uniba.it (ВЗ); stefano.pavan@uniba.it (СП)
- 2 Кафедра наук о сельском хозяйстве, продовольствии и окружающей среде, Университет Фоджи, Via Napoli 25, 71122 Фоджа, Италия
- 3 Кафедра биологических наук, биотехнологий и биофармацевтики, Университет Бари, Via Orabona 4, 70125 Бари, Италия; guglielmo.rainaldi@uniba.it
- 4 Департамент энергетических технологий, отдел биоэнергетики, биопереработки и зеленой химии, Исследовательский центр ENEA Trisaia, SS 106 Ionica, км 419+500, 75026 Ротонделла (MT), Италия; paolo.iovieno@enea.it
* Переписка: rosa.mazzeo@unifg.it (РМ); concetta.lotti@unifg.it (КЛ)
Абстрактные:
Лук (Аллиум сера L.) является второй по значимости овощной культурой в мире и широко ценится за свою пользу для здоровья. Несмотря на свою значительную экономическую значимость и ценность в качестве функционального продукта питания, лук плохо исследован на предмет его генетического разнообразия. Здесь мы исследовали генетическую изменчивость «красного лука Acquaviva» (ARO), местного сорта с вековой историей выращивания в небольшом городке в провинции Бари (Апулия, юг Италии). Набор из 11 микросателлитных маркеров был использован для изучения генетических вариаций в коллекции зародышевой плазмы, состоящей из 13 популяций ARO и трех распространенных коммерческих типов. Анализ генетической структуры с помощью параметрических и непараметрических методов показал, что ARO представляет собой четко определенный генофонд, явно отличающийся от местных сортов Тропеа и Монторо, с которыми его часто путают. Чтобы дать описание луковиц, обычно используемых для потребления в свежем виде, оценивали содержание растворимых твердых веществ и остроту, показавшие более высокую сладость в ARO по сравнению с двумя вышеупомянутыми местными сортами. В целом, настоящее исследование полезно для будущего повышения ценности ARO, чему можно было бы способствовать с помощью маркировки качества, которая могла бы способствовать ограничению коммерческого мошенничества и повышению доходов мелких землевладельцев.
Введение
Род Allium насчитывает около 750 видов [1], среди которых одним из наиболее распространенных является лук (Allium cepa L., 2n = 2x =16). A. cepa имеет двухгодичный цикл и ауткроссинговое репродуктивное поведение. В настоящее время мировое производство лука (97.9 млн тонн) делает его второй по значимости овощной культурой после томата [2]. Луковицы лука издревле использовались как в пищу, так и в народных лечебных целях. Действительно, древние египтяне уже сообщили о нескольких терапевтических формулах, основанных на использовании чеснока и лука, в медицинском папирусе 1550 г. до н. э., Кодексе Эберса [3].
Этот универсальный и полезный овощ употребляют в сыром, свежем или переработанном виде и используют для улучшения вкуса многих блюд. Несколько недавних исследований утверждают, что потребление лука может снизить риск сердечно-сосудистых заболеваний [4,5], ожирения [6], диабета [7] и различных форм рака [8–10]. Полезные свойства лука часто объясняются высоким содержанием двух классов нутрицевтических соединений: флавоноидов и алк(ен)илцистеинсульфоксидов (АКСО). К первому классу относятся флавонолы и антоцианы. Кверцетин является основным обнаруживаемым флавонолом, известным своими сильными антиоксидантными и противовоспалительными свойствами в отношении удаления свободных радикалов и связывания ионов переходных металлов. [11]; тогда как антоцианы придают красный/фиолетовый цвет некоторым сортам лука. Что касается ACSO, то наиболее распространенным является изоаллиин [(+)-транс-S-1-пропенил-L-цистеинсульфоксид] [12], запасаемая в клетках нелетучая и непротеиногенная серная аминокислота, которая косвенно отвечает за острый аромат и вкус лука. [13]. При разрушении тканей изоаллиин расщепляется ферментом аллииназой с образованием ряда летучих соединений (пируват, аммиак, тиосульфонаты и пропанетиальный S-оксид), которые вызывают слезотечение и вызывают неприятный запах (острость). [14]. Остроту лука часто измеряют количеством на грамм сырого веса пировиноградной кислоты, образующейся в результате гидролиза. [15, 16].
В странах Средиземноморского бассейна, предложенных в качестве одного из вторичных центров разнообразия А. сепа [17, 18]Луковицы лука сильно различаются по форме, размеру, цвету, сухому веществу и остроте. [19-22:XNUMX]. Кроме того, удобрения на основе серы, агрономические приемы, тип почвы, климатические условия и генотип сортов или местных сортов могут влиять на качество луковиц, придавая им особые органолептические и питательные свойства. [23-27:XNUMX]. В Италии, несмотря на широкую доступность зародышевой плазмы лука, лишь несколько сортов лука часто подвергаются научным исследованиям и должным образом охарактеризуются. [28, 29].
Тщательная генетическая и фенотипическая характеристика агробиоразнообразия имеет решающее значение для обеспечения надлежащего сохранения генетических ресурсов растений и содействия использованию конкретных генотипов в цепочке создания стоимости. [30-32:XNUMX]. Для картирования часто выбирались маркеры простых повторов последовательности (SSR). [33-35:XNUMX], дактилоскопия ДНК и дискриминация сортов [36-38:XNUMX]и надежная оценка генетической изменчивости внутри местных сортов и между ними. [39-42:XNUMX], поскольку они локус-специфичны, мультиаллельны, кодоминантно наследуются, высоко воспроизводимы и подходят для автоматического генотипирования.
В настоящем исследовании мы сосредоточили наше внимание на традиционном апулийском староместном сорте «Красный лук Аквавива» (ARO), который выращивается в соответствии с методами органического земледелия на небольшой территории города Аквавива-делле-Фонти, провинция Бари. (Апулия, Южная Италия). Луковицы этого местного сорта большие, приплюснутые, красного цвета и широко используются в местных рецептах. Хотя ARO получила знак качества «Президиум Слоу Фуд», ее производство могло бы и дальше продвигаться и защищаться знаками качества Европейского Союза, такими как защищенное географическое указание (PGI) и защищенное наименование происхождения (POD), поскольку они могут способствовать ограничению коммерческое мошенничество и повысить доходы мелких землевладельцев. В данном случае молекулярные маркеры SSR использовались в качестве мощных инструментов для оценки генетической изменчивости среди популяций ARO и для различения этого стародавнего сорта от двух других южноитальянских староместных сортов красного лука. Кроме того, мы оценили остроту и содержание растворимых твердых веществ, чтобы оценить вкус ARO в зависимости от рыночного спроса.
Итоги
Создание коллекции зародышевой плазмы красного лука Acquaviva и морфологическая характеристика
Семена 13 популяций староместного сорта ARO, подаренные фермерами в рамках проекта BiodiverSO в регионе Апулия, были использованы для создания коллекции зародышевой плазмы ARO.
Морфологические дескрипторы, относящиеся к луковице, кожице и мякоти, были собраны на зародышевой плазме ARO и на трех местных сортах лука, два из которых принадлежали старому сорту «Красный лук Тропеа» (TRO), а один — старому сорту «Монторо медный лук» (MCO) (рисунок). 1). Все луковицы ARO были плоскими и имели красную внешнюю кожуру и мякоть разных оттенков красного. Напротив, мякоть луковиц TRO была полностью красной, тогда как мякоть луковиц MCO была плохо пигментирована (Таблица S1). Биохимический анализ позволил оценить содержание твердых растворимых веществ и остроту. Как сообщается в таблице 1, средние значения содержания твердых растворимых веществ в луковицах в популяциях ARO составляли 7.60 и колебались от 6.00 (ARO12) до 9.50° Брикса (ARO11 и ARO13). Это значение было выше, чем рассчитанное для местных сортов TRO и MCO (4.25 и 6.00° Брикса соответственно).

Таблица 1. Содержание твердых растворимых веществ и значения остроты, оцененные в популяциях «Acquaviva Red Onion» (ARO), «Tropea Red Onion» (TRO) и «Montoro Copper Onion» (MCO) *.
| КОД | Растворимое твердое содержание (по шкале Брикса) | Острота (pмолг–1 ФВ) | ||
| среднее | CV y (%) | среднее | CV y (%) | |
| АРО1 | 6.25 Д * | 5.65 | 5.84 аб * | 23.78 |
| АРО2 | 7.25 DC | 4.87 | 6.51 в | 22.98 |
| АРО3 | 7.50 BCD | 9.42 | 5.28 пр. | 22.88 |
| АРО4 | 7.50 BCD | 0.00 | 6.97 в | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 в | 9.68 |
| АРО6 | 6.25 D | 5.65 | 4.51 пр. | 39.18 |
| АРО7 | 7.25 DC | 4.87 | 5.25 пр. | 15.44 |
| АРО8 | 9.00 AB | 0.00 | 7.04 в | 3.49 |
| АРО9 | 8.25 азбука | 4.28 | 6.84 в | 0.15 |
| АРО10 | 7.00 DC | 0.00 | 5.94 пр. | 6.57 |
| АРО11 | 9.50 | 7.44 | 5.54 пр. | 16.43 |
| АРО12 | 6.00 D | 0.00 | 4.91 пр. | 9.70 |
| АРО13 | 9.50 | 7.44 | 6.63 в | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 пр. | 2.66 |
| ТРО1 | 4.25 E | 8.31 | 2.80 б | 2.10 |
| ТРО2 | 4.25 E | 8.31 | 4.28 пр. | 4.79 |
* Средние значения с одинаковыми буквами в верхнем или нижнем регистре статистически не различаются при 0.01P или 0.05P соответственно (тест СНК). y Коэффициент вариации.
Среднее значение остроты ARO, оцененное по содержанию пировиноградной кислоты, составило 6.00 и варьировалось от 4.51 пмоль г.-1 от прошивки (ARO6) до 7.04 (ARO8). Это значение было выше, чем рассчитанное для местных сортов TRO и MCO (3.54 пмоль г).-1 FW и 4.18 пмоль г-1 FW соответственно).
SSR-полиморфизм и генетические связи между образцами
В настоящем исследовании 11 из 37 протестированных комбинаций праймеров SSR обеспечивали однолокусный полиморфизм, т.е. давали не более двух продуктов амплификации у одного индивидуума. Всего у 55 особей выявлено 320 аллелей с числом аллелей на локус от 2 (ACM147 и ACM 504) до 11 (ACM132) и средним значением 5 аллелей (табл. 2). В отдельных популяциях число аллелей (Na) колебалось от 1.94 (ACM147 и ACM504) до 5.38 (ACM132), тогда как эффективное число аллелей (Ne) колебалось от 1.41 (ACM152) до 2.82 (ACM449). Расхождения Между значениями Na и Ne объяснялись наличием в популяциях аллелей с низкой частотой и преобладанием лишь нескольких аллелей. Наибольшее наблюдаемое значение гетерозиготности (Ho) было отмечено для ACM138 и ACM449 (0.62), тогда как самое низкое было связано с ACM152 (0.25). Ожидаемая гетерозиготность (He), которая соответствует теоретическому ожиданию в панмиктической популяции, колебалась от 0.37 (ACM504) до 0.61 (ACM132, ACM138 и ACM449). Индекс фиксации Райта (Fis) отображал значения, близкие к нулю (в среднем 0.05) для всех маркеров, что указывает на схожие значения между наблюдаемым и ожидаемым уровнями гетерозиготности, как и ожидалось для ауткроссирующего вида. Эффективность отдельного маркера SSR в генетическом фингерпринтинге оценивалась по индексу содержания полиморфной информации (PIC), среднее значение которого составляло 0.48 и колебалось от 0.33 (ACM504) до 0.67 (ACM132). Другой индекс эффективности, информационный индекс Шеннона (I), имел среднее значение 0.84, а предполагаемые значения варьировались от 0.45 (ACM152) до 1.20 (ACM132).
Таблица 2. Особенности полиморфизма 11 маркеров SSR, используемых для оценки генетического разнообразия в популяциях ARO, TRO и MCO. Общее количество аллелей (Na), диапазон размеров полос и индекс содержания полиморфной информации (PIC). См. общую выборку из 320 человек, генотипированных в этом исследовании. Число аллелей (Na), количество эффективных аллелей (Ne), наблюдаемая гетерозиготность (Ho), ожидаемая гетерозиготность (He), индекс фиксации (Fis), а информационный индекс Шеннона (I) относится к средним значениям, рассчитанным на основе 16 популяций, каждая из которых состоит из 20 человек.
| Локус. | Всего Na | Диапазон размеров (п.п.) | ПИК | среднее | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| среднее | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Среди популяций ARO3, ARO6, ARO8, ARO10, TRO1 и MCO демонстрировали высокий уровень генетической изменчивости (Ho > 0.5), тогда как наименьшее разнообразие наблюдалось в популяции ARO7 (Ho = 0.27) (дополнительная таблица S2). В целом все образцы имели Fis значения, близкие к нулю (Fis среднее значение = 0.054), как и ожидалось при случайных условиях спаривания.
Анализ молекулярной дисперсии и генетической структуры
Иерархическое распределение генетических вариаций между популяциями и внутри них было рассчитано с помощью AMOVA. Результаты выявили значительную долю генетических вариаций внутри популяций (87%). Вариации среди популяций, 13%, были весьма значительными (P < 0.001) (Таблица 3). Значимыми были парные значения параметра Fpt, аналога индекса фиксации Fst Райта, в пределах от 0.002 (ARO2/ARO10) до 0.468 (ARO7/TRO2) (P <0.05), за исключением девяти парных сравнений (дополнительная таблица S3).
Таблица 3. Анализ молекулярной дисперсии 320 генотипов из 16 популяций Allium сера L.
| Источник | df | Сумма квадратов | Оценка дисперсии | Дисперсия (%) | Fpt | P |
| Среди населения | 15 | 458.63 | 1.16 | 13% | ||
| Внутри популяций | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Всего | 319 | 2731.62 | 8.66 |
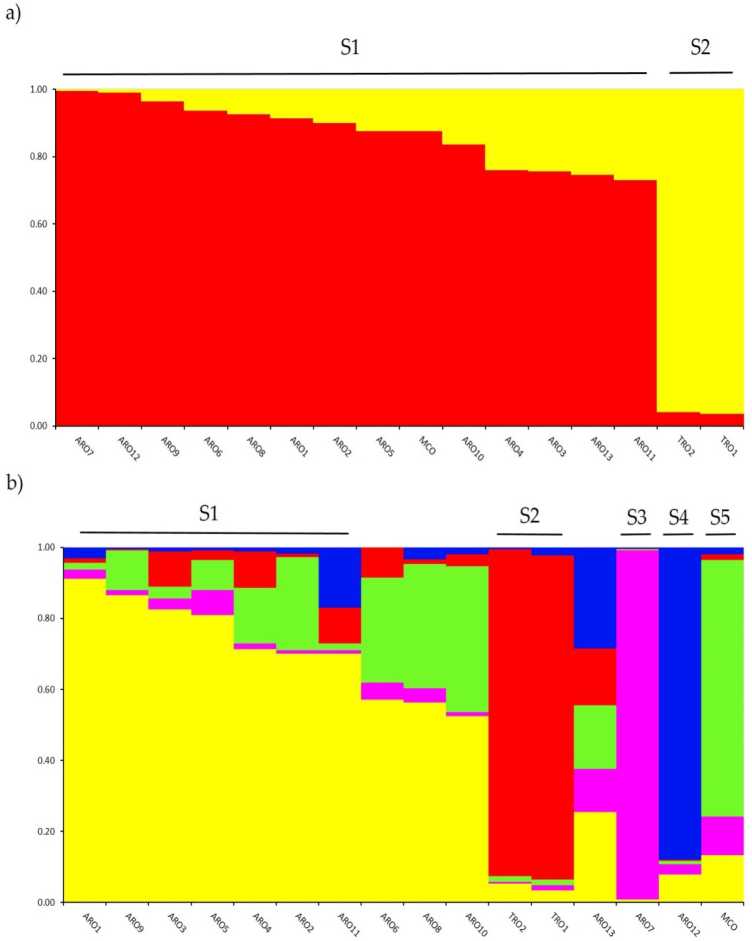
Исследование генетической структуры в А. сепа коллекцию, генотипированную в этом исследовании, выполняли с помощью кластерного анализа на основе модели примесей, реализованного в программном обеспечении STRUCTURE. Метод Эванно А.К. предполагал разделение на два кластера (К = 2) как наиболее информативное для наших исследований. Набор данных,с тe следующий самый высокий рейтингок в К = 5 (дополнение к тексту С1), для К = 2, aл.с.opуляции спрежде чем задницаigned слишкомnоf два кластера коэффициент rnernbertoip (q) > 0.7. Как сhoвошел в фигура 2a, первый кластер (названный S1) включал MCO и все популяции ARO, тогда как кластер S2 группировал две популяции TRO. При K = 5, что обеспечивает более глубокое описание набора данных (рис. 2b), 75% образцов отнесены к одному из пяти кластеров. Разделение между ARO (S1) и TRO (S2) было подтверждено, хотя некоторые популяции ARO были смешаны (q <0.7) или сгруппированы отдельно в два новых кластера S3 и S4 (ARO7 и ARO12 соответственно). Интересно, что коммерческий тип MCO образовал отдельный кластер (S5), отделенный от апулийского красного лука.
Генетические связи между популяциями
Полиморфизм SSR позволил построить дендрограмму генетического разнообразия, а результаты филогенетического анализа представлены на рисунке. 3a. Здесь коллекция зародышевой плазмы была разделена на пять групп, сильно поддерживаемых бутстреп-ценностями. Популяции ARO7 и ARO12 были немедленно отделены от остальных популяций и образовали два отдельных кластера. Третий кластер включал две коммерческие популяции TRO, тогда как четвертый узел отделял MCO от одиннадцати популяций ARO. Генетические взаимоотношения, возникающие между популяциями, были дополнительно исследованы с помощью анализа главных координат (PCoA) (рис. 3b). Как подчеркивалось ранее, популяции ARO были плотно сгруппированы, за исключением ARO12 и ARO7, которые появлялись в изолированных позициях на графике PCoA. Два TRO и популяции MCO были разбросаны в правом нижнем углу графика.
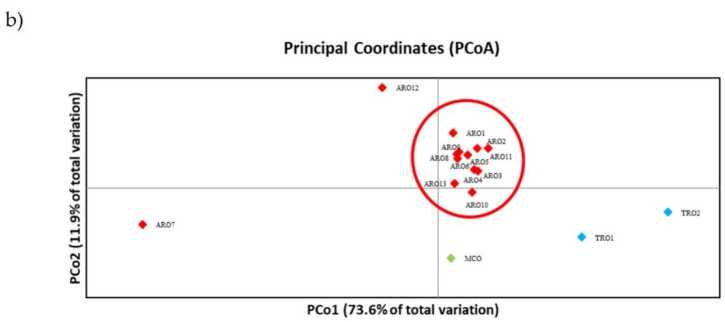
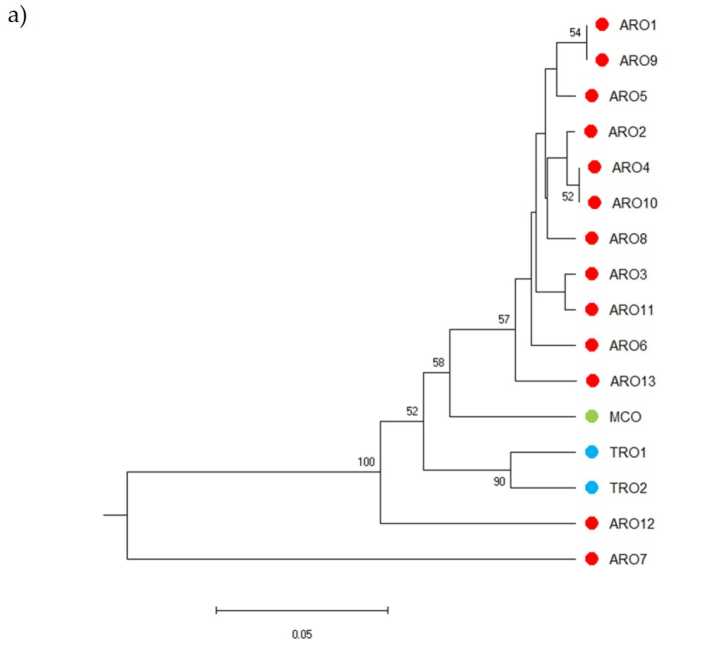
Рисунок 3. Генетическое разнообразие среди 16 А. сепа популяции, охарактеризованные в этом исследовании на основе их профиля ССР. (a) UPGMA-дендрограмма генетической дистанции. Значения поддержки начальной загрузки >50 указаны над соответствующими узлами; (b) анализ главных компонент (PCoA). Кластер, обведенный красным, полностью соответствует группе, полученной в результате филогенетического анализа и состоящей из 11 образцов ARO.
Обсуждение
Среди большого количества агробиоразнообразия, традиционно культивируемого на юге Италии, местные сорта лука представляют собой нишевые продукты, которые необходимо сохранить от риска генетической эрозии и угрозы замены современными сортами. В рамках регионального проекта BiodiverSO, направленного на сбор, характеристику, продвижение и охрану генетических ресурсов региона Апулия, тесно связанных с местным наследием, мы создали коллекцию семян из 13 популяций местных сортов ARO. Мы сообщили о первой оценке вариаций ARO с точки зрения полиморфизма ДНК и двух биохимических параметров, содержания растворимых твердых веществ и пировиноградной кислоты, связанных с вкусовыми характеристиками и важных для восприятия свежих сырых продуктов. Кроме того, данные по старому сорту ARO сравнивались с данными, собранными по двум другим староместным сортам пигментированного лука, с которыми часто ошибались.
Биохимический анализ выявил сладость 13 популяций ARO, связанную с высоким содержанием растворимых твердых веществ и средней остротой, в соответствии с рекомендациями отрасли сладкого лука. [31]. Луковицы ARO были слаще, чем луковицы местных сортов TRO и MCO, и имели немного более высокую остроту. Однако сладость лука обусловлена балансом между содержанием сахара и остротой, поэтому эта характеристика может быть полезна для выбора ценных генотипов, который обычно проводится фермерами только на основе морфологии.
Было подтверждено, что маркеры SSR являются полезным инструментом для распознавания генотипов, хотя они собраны на узкой растущей территории, такой как город Аквавива-делле-Фонти. Выбранные маркеры отображали большее количество аллелей, чем маркеры, о которых ранее сообщалось [43] и [44], но ниже, чем маркеры, сообщенные [45]. Более того, 50% нашего набора маркеров показали значения индекса PIC более 0.5, что оказалось пригодным для дискриминации популяций в коллекции, как предполагает [46]. Оценка разнообразия внутри популяций выявила схожие значения между Ho и He, что привело к низкому Fi.s ценности. Это согласуется с ауткроссинговым характером А. цепа, который серьёзно страдает инбредной депрессией [47]. Общий Фиs Значение, рассчитанное для популяций лука, рассматриваемых в этом исследовании (0.054), было ниже, чем ранее сообщенное [45] (0.22) и практически идентично найденному [31] (0.08) и [48] (0.00), которые оценивали генетическое разнообразие местных сортов лука с северо-запада Испании и Нигера соответственно. Примечательные уровни гетерозиготности в популяциях ARO подтверждают представление о том, что Апулия представляет собой центр разнообразия многих садоводческих видов. [32, 42, 49-51:XNUMX].
AMOVA подчеркнула, что большая часть молекулярных вариаций в коллекции, генотипированной в этом исследовании, находится внутри популяций. Однако значительная генетическая дифференциация популяций (FPT значения) выявило наличие генетической стратификации. Фактически, хотя наши результаты показали наличие генетического единообразия в большинстве популяций ARO, образующих четко определенный кластер, популяции ARO7 и ARO12 демонстрировали четко выраженный генетический профиль. Этот результат может быть обусловлен разным происхождением семян, используемых двумя фермерами, у которых были собраны популяции. Более того, на основании полученных результатов можно считать, что местный сорт ARO явно отличается на генетическом уровне от местных сортов TRO и MCO. В недавнем исследовании [29] оценили генетическое разнообразие нескольких местных сортов итальянского лука, включая «Аквавива», «Тропеа» и «Монторо». Хотя авторы использовали SNP-маркеры для оценки генетического разнообразия более широкой коллекции лука, генотипирование не позволило отличить «Acquaviva» от лука «Tropea» и «Montoro». Вероятно, такое расхождение связано с низким найденным средним значением PIC (0.292), что позволяет предположить умеренную общую информативность анализируемых локусов, как утверждают авторы. [29]. Более того, чтобы исследовать наличие субструктуры в их итальянском кластере, было бы лучше проанализировать итальянские генотипы отдельно от остальной части коллекции. Вероятно, это позволило бы визуализировать структуру генетического разнообразия, связанную с географической стратификацией или признаками эмпирического отбора.
В заключение, настоящее исследование представляет собой всесторонний отчет о староместном сорте лука, связанном с местным культурным наследием и имеющем экономическое значение для фермеров. Наши результаты подчеркивают, что, за некоторыми исключениями, ARO характеризуется четко определенным генофондом, который заслуживает защиты от риска генетической эрозии. Поэтому создание репрезентативной коллекции этого ценного источника генетического разнообразия имело решающее значение. Наконец, генетическая и фенотипическая характеристика ARO может быть полезна для получения знаков качества Европейского Союза.
Материалы и методы
Сбор зародышевой плазмы, растительного материала и экстракция ДНК
Набор из 13 популяций староместных сортов ARO был получен в рамках проекта региона Апулия (BiodiverSO: https://www.biodiversitapuglia.it/), посредством серии миссий, выполненных в «Аквавива делле Фонти», небольшом апулийском городке в провинции Бари, Италия. Места сбора каждого образца были нанесены на карту с помощью Географической информационной системы (ГИС) и представлены в таблице. 4. Кроме того, две популяции местного сорта TRO и одна популяция местного сорта MCO были включены в настоящее исследование и использованы в качестве эталонов. Весь растительный материал выращивался в одинаковых условиях окружающей среды на экспериментальной ферме «П. Мартуччи» Университета Бари (41°1'22.08″ с.ш., 16°54'25.95″ в.д.), под защитным клеткой, чтобы избежать перекрестного опыления между растениями. популяций и обеспечение внутрипопуляционного опыления с помощью мясных мух. (Люсилия Цезарь). 16 популяций были охарактеризованы по признакам, связанным с размером и формой луковицы, а также цветом кожицы и мякоти (Таблица S1). Кроме того, анализ содержания твердых растворимых веществ проводился с использованием ручного рефрактометра и измерялась острота образцов лукового сока с добавлением 2,4-динитрофенилгидразина (0.125% v/v в 2 н. HCl) и оценивая поглощение при 420 нм, как сообщает [31]. Для определения наличия значимых различий были проведены многодиапазонный тест Дункана и тест СНК.
Таблица 4. Список популяций, собранных и генотипированных в этом исследовании. Для каждой популяции сообщается идентификационный код, местное название, координаты GPS и генный банк, сохраняющий семена.
| Code | Фамилия | GPS координаты | Генный банк y |
| АРО1 | Чиполла Росса ди Аквавива | 40°54’21.708″ N 16°49’1.631” E | Ди.ССПА |
| АРО2 | Чиполла Росса ди Аквавива | 40°53’14.28″ N 16°48’56.879” E | Ди.ССПА |
| АРО3 | Чиполла Росса ди Аквавива | 40°54’11.304″ N 16°49’13.079” E | Ди.ССПА |
| АРО4 | Чиполла Росса ди Аквавива | 40°54’3.348″ N 16°40’27.011” E | Ди.ССПА |
| АРО5 | Чиполла Росса ди Аквавива | 40°51’59.76″ N 16°53’0.527” E | Ди.ССПА |
| АРО6 | Чиполла Росса ди Аквавива | 40°52’48.72″ N 16°49’43.247” E | Ди.ССПА |
| АРО7 | Чиполла Росса ди Аквавива | 40°53’13.47″ N 16°50’23.783” E | Ди.ССПА |
| АРО8 | Чиполла Росса ди Аквавива | 40°53’18.816″ N 16°49’33.888” E | Ди.ССПА |
| АРО9 | Чиполла Росса ди Аквавива | 40°54"51.372″ Н 16°49"3.504 E | Ди.ССПА |
| АРО10 | Чиполла Росса ди Аквавива | 40°54’1.188″ N 16°49’24.311” E | Ди.ССПА |
| АРО11 | Чиполла Росса ди Аквавива | 40°52"49.8″ Н 16°49"48.575 E | Ди.ССПА |
| АРО12 | Чиполла Росса ди Аквавива | 40°52’38.892″ N 16°49’28.379” E | Ди.ССПА |
| АРО13 | Чиполла Росса ди Аквавива | 40°53’21.768″ N 16°49’29.711” E | Ди.ССПА |
| ТРО1 | Чиполла Росса Лунга в Тропее | – | Ди.ССПА |
| ТРО2 | Чиполла Росса Тонда ди Тропеа | – | Ди.ССПА |
| MCO | Чиполла Рамата ди Монторо | – | Ди.ССПА |
| y Di.SSPA, факультет почвоведения, растений и пищевых наук, Университет Бари. |
Листовой материал 20 генотипов на популяцию отбирали и хранили при -80°C до использования. Для видов, богатых полисахаридами, например А. цепа, Первые шаги по удалению полисахарида необходимы для получения ДНК хорошего качества, поэтому первоначальные промывки в буфере STE (0.25 М сахароза, 0.03 М Трис, 0.05 М ЭДТА) выполнялись, как описано [52]. Тотальную ДНК экстрагировали методом CTAB. [53] и, наконец, его качество и концентрацию проверяли с помощью УФ-Видимого спектрофотометра Nano Drop 2000 (ThermoScientific, Уолтем, Массачусетс, США) и электрофореза в 0.8% агарозном геле.
Анализ ССР
16 комбинаций праймеров EST-SSR, разработанных [54] и ранее проверено в исследованиях генетического разнообразия [43] и [44] и 21 геномный ССР [45-55:XNUMX] были проверены для оценки их пригодности (дополнительная таблица S4). Генотипирование проводили с использованием метода экономичной флуоресцентной маркировки, при котором хвост M13 добавляется к каждому прямому праймеру SSR. [56]. Смеси для ПЦР готовили в реакционной смеси объемом 20 г, содержащей: 50 нг тотальной ДНК, 0.2 мМ смеси dNTP, 1X реакционного буфера для ПЦР, 0.8 ед. ДНК-полимеразы DreamTaq (Thermo Scientific, Уолтем, Массачусетс, США), 0.16 гМ обратного праймера. , 0.032 г прямого праймера, удлиненного последовательностью M13 (5'-TGTAAAACGACGGCCAGT-3'), и 0.08 гМ универсального праймера M13, меченного флуоресцентными красителями FAM или NED (Sigma-Aldrich, Сент-Луис, Миссури, США). Реакции ПЦР проводили в термоциклере SimpliAmp (Applied Biosystems, Калифорния, США) при следующих условиях для большинства пар праймеров: 94 °С в течение 5 мин, 40 циклов при 94 °С в течение 30 с, 58 °С. в течение 45 с и 72 °С в течение 45 с и финальная элонгация при 72 °С в течение 5 мин. Что касается ACM446 и ACM449, применяли тачдаун-ПЦР с отжигом от 60°C до 55°C в течение 10 циклов, 30 циклов при 55°C, с последующим окончательным продлением в течение 5 минут при 72°C. Продукты ПЦР загружали в 96-луночный планшет и смешивали с 14 г Hi-Di формамида (Life Technologies, Карлсбад, Калифорния, США) и 0.5 г GeneScan 500 ROX Size Standard (Life Technologies, Карлсбад, Калифорния, США). Ампликоны разделяли с помощью капиллярного секвенатора ABI PRISM 3100 Avant Genetic Analyser (Life Technologies, Карлсбад, Калифорния, США), где аллели оценивали как кодоминантные и присваивали их с помощью программного обеспечения GeneMapper версии 3.7.
Программное обеспечение GenAlEx 6.5. [57] и Цервус 3.0.7 [58] были использованы для оценки количества аллелей (Na), количества эффективных аллелей (Ne), наблюдаемой гетерозиготности (Ho), ожидаемой гетерозиготности (He), содержания полиморфной информации (PIC), информационного индекса Шеннона (I) и индекса фиксации (Fis). ) для каждого локуса SSR.
Оценка генетического разнообразия
Иерархическое разделение генетических вариаций между популяциями лука и внутри них оценивалось с помощью GenAlEx 6.5. [57] посредством анализа молекулярной дисперсии (AMOVA) с бутстрэппингом 999 для проверки значимости. Кроме того, программное обеспечение GenAlEx 6.5 использовалось для оценки разнообразия внутри каждой популяции путем расчета среднего значения Ho, He и Fis по всем локусам SSR.
Структура населения была получена с помощью алгоритма кластеризации на основе байесовской модели, реализованного в программном обеспечении STRUCTURE v.2.3.4. [59]. Набор данных обрабатывался с использованием нескольких гипотетических кластеров (K) в диапазоне от 1 до 10, при этом для каждого значения K было задано десять независимых прогонов. Для каждого запуска с целью проверки согласованности результатов было выполнено 100,000 100,000 начальных периодов приработки и XNUMX XNUMX итераций Марковской цепи Монте-Карло (MCMC) в рамках модели примеси и независимых частот аллелей среди популяций. Наиболее вероятное значение K было определено с использованием метода AK, описанного [60], в веб-программе STRUCTURE HARVESTER [61]. Отдельную популяцию относили к определенному кластеру, когда ее коэффициент принадлежности (значение q) превышал 0.7, в противном случае ее считали смешанной.
Анализ основных координат был проведен для того, чтобы визуализировать закономерности генетического родства между образцами, выявленные с помощью матрицы генетических расстояний Нея (дополнительная таблица S5). На основании частот аллелей была построена дендрограмма генетической дистанции с применением кластерного анализа невзвешенных парных групп (UPGMA) в программе POPTREEW. [62]. Для оценки достоверности иерархической кластеризации применялась бутстрэппинг с установкой 100 повторной выборки набора данных. Наконец, программное обеспечение MEGA X [63] использовался в качестве программного обеспечения для рисования деревьев.
Дополнительные материалы: Следующее доступно онлайн на http://www.mdpi.com/2223-7747/9/2/260/s1. Таблица S1: Морфологическая характеристика луковиц ARO, MCO и TRO. Таблица S2: Индексы гетерозиготности и фиксации, рассчитанные для местных сортов ARO и местных сортов TRO и MCO. Таблица S3: Парные значения параметра Fpt. Таблица S4: Список SSR, использованных в исследовании. Таблица S5. Попарная популяционная матрица генетического расстояния Нея. Рисунок S1: Линейный график изменения значений K в зависимости от дельты K Эванно.
Авторские вклады: CL и LR задумали исследование и разработали эксперимент; CL и PI провели анализ молекулярных маркеров; АРМ и ВЗ провели полевые испытания; RM, SP, GR и CL участвовали в анализе данных; RM и CL написали рукопись. Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование: Эта работа финансировалась региональным апулийским проектом «Биоразнообразие апулийских видов овощей» — Programma di Sviluppo Rurale per la Puglia 2014-2020. Мисура 10 – Соттомисура 10.2; грант CUP H92C15000270002, Италия.
Подтверждения: Благодарность выражается компаниям «Azienda Agricola Iannone Anna» и «Associazione produttori della vera cipolla rossa di Acquaviva» за предоставление растительных материалов, использованных в эксперименте.
Конфликт интересов: Авторы объявили, что нет никаких конфликтов интересов.
Рекомендации
- 1. Стерн, В.Т. Сколько видов лука известно? Кью Мэг. 1992, 9, 180-182. [CrossRef]
- 2. ФАОСТАТ. Статистическая база данных ФАО. Доступно онлайн: http://www.fao.org/2017 (по состоянию на 8 января 2019 г.).
- 3. Блок Э. Химия чеснока и лука. Sci. Am. 1985, 252, 114-119. [CrossRef]
- 4. Ли, Б.; Юнг, Дж. Х.; Ким, Х.С. Оценка антиоксидантной активности красного лука у крыс. Пищевая хим. Токсикол. 2012, 50, 3912-3919. [CrossRef]
- 5. Ли, С.М.; Мун, Дж.; Чунг, Дж. Х.; Ча, YJ; Шин, М.Дж. Влияние экстрактов луковой шелухи, богатых кверцетином, на артериальный тромбоз у крыс. Пищевая хим. Токсикол. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Ёсинари, О.; Сиодзима, Ю.; Игараси, К. Действие экстракта лука на ожирение у жирных крыс с сахарным диабетом. Питательные вещества 2012, 4,1518-1526. [CrossRef]
- 7. Акаш, МСХ; Рехман, К.; Чен, С. Пряное растение Allium cepa: пищевая добавка для лечения сахарного диабета 2 типа. Питание 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Ван Ю.; Тянь, Западная X; Ma, XF ингибирующее действие лука (Аллиум сера L.) экстракт влияет на пролиферацию раковых клеток и адипоцитов посредством ингибирования синтазы жирных кислот. Азиатский Пак. Дж. Рак Пред. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Лай, WW; Сюй, Южная Каролина; Чуэ, ФС; Чен, ГГ; Ян, Дж. С.; Лин, JP; Лиен, Дж. К.; Цай, CH; Чунг, Дж. Г. Кверцетин ингибирует миграцию и инвазию клеток рака полости рта человека SAS посредством ингибирования сигнальных путей NF-kappaB и матриксной металлопротеиназы-2/-9. Противораковый Res. 2013, 33, 1941-1950. [PubMed]
- 10. Никастро, Х.Л.; Росс, ЮАР; Милнер, Дж. Чеснок и лук: их свойства профилактики рака. Рак Пред. Местожительство 2015, 8,181-189. [CrossRef]
- 11. Форте, Л.; Торричелли, П.; Боанини, Э.; Газзано, М.; Рубини, К.; Фини, М.; Биги, А. Антиоксидантные и восстановительные свойства гидроксиапатита, функционализированного кверцетином: исследование совместной культуры остеобластов, остеокластов и эндотелиальных клеток in vitro. Акта Биоматер. 2016, 32, 298-308. [CrossRef]
- 12. Ямадзаки, Ю.; Ивасаки, К.; Миками, М.; Ягихаши, А. Распределение одиннадцати предшественников вкуса, производных S-алк(ен)ил-L-цистеина, в семи овощах лука. Пищевая наука. Технол. Рез. 2011, 17, 55-62. [CrossRef]
- 13. Блок, Э. Сероорганическая химия рода Allium. Значение для органической химии серы. Энгью. Chem. Int. Эд. Англ. 1992, 31, 1135-1178. [CrossRef]
- 14. Гриффитс, Г.; Труман, Л.; Кроутер, Т.; Томас, Б.; Смит, Б. Лук – глобальная польза для здоровья. Фитотер. Рез. 2002,16, 603-615. [CrossRef]
- 15. Швиммер, С.; Уэстон, У.Дж. Ферментативное выделение пировиноградной кислоты в луке как показатель остроты. Дж. Агрик. Пищевая хим. 1961, 9, 301-304. [CrossRef]
- 16. Кеттер, Кэт; Рэндл, В.М. Оценка остроты лука. В Проверенные исследования для лабораторного обучения; Керхер, С.Дж., Ред.; Ассоциация биологического лабораторного образования (ABLE): Нью-Йорк, штат Нью-Йорк, США, 1998 г.; Том 19, стр. 177–196.
- 17. Ханельт П. Таксономия, эволюция и история. В Лук и родственные культуры, Том. I. Ботаника, физиология и генетика; Рабинович, Х.Д., Брюстер, Дж.Л., ред.; CRC Press: Бока-Ратон, Флорида, США, 1990; стр. 1-26.
- 18. Рабинович, Х.Д.; Курра, Л. Наука о выращивании лука: последние достижения; Издательство CABI: Уоллингфорд, Великобритания, 2002 г.
- 19. Мэллор, К.; Карраведо, М.; Эстопанан, Г.; Мэллор, Ф. Характеристика генетических ресурсов лука (Аллиум сера Л.) из испанского вторичного центра разнообразия. Охватывать. Дж. Агрик. Рез. 2011, 9, 144-155. [CrossRef]
- 20. Фериоли, Ф.; Д'Антуоно, Л.Ф. Оценка фенольных соединений и сульфоксидов цистеина в местной зародышевой плазме лука и лука-шалота из Италии и Украины. Жене. Ресурс. Кроп Эвол. 2016, 63, 601-614. [CrossRef]
- 21. Петропулос, С.А.; Фернандес, А.; Баррос, Л.; Феррейра, ICFR; Нтаци, Г. Морфологическое, пищевое и химическое описание «ватикиотико», местного местного сорта лука из Греции. Пищевая хим. 2015,182, 156-163. [CrossRef]
- 22. Лигуори, Л.; Адилетта, Г.; Наззаро, Ф.; Фратианни, Ф.; Ди Маттео, М.; Альбанезе, Д. Биохимические, антиоксидантные свойства и антимикробная активность различных сортов лука в Средиземноморье. J. Измерения продуктов питания. Характер. 2019,13, 1232-1241. [CrossRef]
- 23. Ю, КС; Пайк, Л.; Кросби, К.; Джонс, Р.; Лесковар, Д. Различия в остроте лука в зависимости от сортов, условий роста и размеров луковиц. наук. Хортик. 2006,110, 144-149. [CrossRef]
- 24. Беск, Н.; Пернер, Х.; Шварц, Д.; Джордж, Э.; Кро, Л.В.; Рон, С. Распределение кверцетин-3, 4'-O-диглюкозида, кверцетин-4'-O-моноглюкозида и кверцетина в разных частях луковицы лука (Allium cepa L.) под влиянием генотипа. Пищевая хим. 2010,122, 566-571. [CrossRef]
- 25. Карузо, Дж.; Конти, С.; Виллари, Дж.; Боррелли, К.; Мельчионна, Г.; Минутоло, М.; Руссо, Г.; Амальфитано, К. Влияние времени пересадки и густоты растений на урожайность, качество и содержание антиоксидантов в луке. (Аллиум сера Л.) на юге Италии. наук. Хортик. 2014,166, 111-120. [CrossRef]
- 26. Перес-Грегорио, MR; Регейру, Дж.; Симал-Гандара, Дж.; Родригес, А.С.; Алмейда, DPF Повышение добавленной стоимости лука как источника антиоксидантных флавоноидов: критический обзор. Crit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Понл, Т.; Швайггерт, Р.М.; Карл, Р. Влияние метода выращивания и выбора сорта на растворимые углеводы и острые свойства лука (Аллиум сера Л.). Дж. Агрик. Пищевая хим. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Тедеско И.; Карбоне, В.; Спаньоло, К.; Минаси, П.; Руссо, Г.Л. Идентификация и количественная оценка флавоноидов двух южно-итальянских сортов Allium сера L., Tropea (красный лук) и Montoro (медный лук) и их способность защищать эритроциты человека от окислительного стресса. Дж. Агрик. Пищевая хим. 2015, 63, 5229-5238. [CrossRef]
- 29. Виллано, К.; Эспозито, С.; Каруччи, Ф.; Фрушанте, Л.; Карпуто, Д.; Аверсано, Р. Высокопроизводительное генотипирование лука выявляет структуру генетического разнообразия и информативные SNP, полезные для молекулярной селекции. Мол. Порода. 2019, 39, 5. [CrossRef]
- 30. Меркати, Ф.; Лонго, К.; Пома, Д.; Аранити, Ф.; Лупини, А.; Маммано, ММ; Фиоре, MC; Абенаволи, MR; Сансери, F Генетическая вариация итальянского томата длительного хранения. (Solanum lycopersicum L.) сбор с использованием SSR и морфологических признаков плодов. Жене. Ресурс. Кроп Эвол. 2014, 62, 721-732. [CrossRef]
- 31. Гонсалес-Перес, С.; Мэллор, К.; Гарсес-Клавер, А.; Мерино, Ф.; Табоада, А.; Ривера, А.; Помар, Ф.; Перович, Д.; Сильвар, К. Изучение генетического разнообразия и качественных показателей в коллекции лука. (Аллиум сера L.) староместные сорта северо-запада Испании. генетика 2015, 47, 885-900. [CrossRef]
- 32. Лотти, К.; Иовьено, П.; Чентомани, И.; Маркотриджано, Арканзас; Фанелли, В.; Мимиола, Г.; Суммо, К.; Паван, С.; Риккарди, Л. Генетическая, биоагрономическая и пищевая характеристика капусты (Brassica Oleracea Л. вар. acephala) разнообразие в Апулии, Южная Италия. Разнообразие 2018,10, 25. [CrossRef]
- 33. Бардаро, Н.; Маркотриджано, Арканзас; Бракуто, В.; Маццео, Р.; Риккарди, Ф.; Лотти, К.; Паван, С.; Риккарди, Л. Генетический анализ устойчивости к Оробанче Крената (Форск.) в горошине (Pisum посевной L.) линия с низким содержанием стриголактона. Дж. Плант Патол. 2016, 98, 671-675.
- 34. Вако, Т.; Цуказаки, Х.; Ягучи, С.; Ямасита, К.; Ито, С.; Сигё, М. Картирование локусов количественных признаков времени свертывания лука в гроздь (Allium fistulosum Л.). Эуфитика 2016, 209, 537-546. [CrossRef]
- 35. Дакка, Н.; Мухопадхьяй, А.; Паритош, К.; Гупта, В.; Пенталь, Д.; Прадхан, А.К. Идентификация генных SSR и построение карты связей на основе SSR в Брассика юнная. Эвфитика 2017, 213, 15. [CrossRef]
- 36. Анандхан, С.; Моте, СР; Гопал Дж. Оценка сортовой идентичности лука с использованием маркеров SSR. Семеноводство. Технол. 2014, 42, 279-285. [CrossRef]
- 37. Митрова, К.; Свобода, П.; Овесна, Дж. Выбор и проверка набора маркеров для дифференциации сортов лука из Чешской Республики. Чех Я. Жене. Порода растений. 2015, 51, 62-67. [CrossRef]
- 38. Ди Риенцо, В.; Миацци, ММ; Фанелли, В.; Сабетта, В.; Монтемурро, К. Сохранение и характеристика биоразнообразия зародышевой плазмы апулийских оливок. Акта Хортик. 2018,1199,1-6. [CrossRef]
- 39. Мэллор, К.; Арнедо-Андрес, А.; Гарсес-Клавер, А. Оценка генетического разнообразия испанцев Allium сера староместные сорта лука для селекции с использованием микросателлитных маркеров. наук. Хортик. 2014,170, 24-31. [CrossRef]
- 40. Ривера, А.; Мэллор, К.; Гарсес-Клавер, А.; Гарсия-Уллоа, А.; Помар, Ф.; Сильвар, К. Оценка генетического разнообразия лука (Allium сера L.) староместные сорта северо-запада Испании и сравнение с европейской изменчивостью. NZJ Урожай Хортик. 2016, 44, 103-120. [CrossRef]
- 41. Де Джованни, К.; Паван, С.; Таранто, Ф.; Ди Риенцо, В.; Миацци, ММ; Маркотриджано, Арканзас; Манджини, Г.; Монтемурро, К.; Риккарди, Л.; Лотти, К. Генетическая вариация глобальной коллекции зародышевой плазмы нута. (Цицер ариетинум L.), включая итальянские образцы, подверженные риску генетической эрозии. Физиол. Мол. Биол. Растения 2017, 23, 197-205. [CrossRef]
- 42. Маццео, Р.; Моргезе, А.; Соннанте, Г.; Сулуага, ДЛ; Паван, С.; Риккарди, Л.; Лотти, К. Генетическое разнообразие брокколи рабе. (Брассика рапа Л. подвид. обыкновенная (Л.) Янч.) из Южной Италии. наук. Хортик. 2019, 253, 140-146. [CrossRef]
- 43. Джаксе, М.; Мартин, В.; МакКаллум, Дж.; Хэви, М. Однонуклеотидные полиморфизмы, инделы и простые повторы последовательностей для идентификации сортов лука. Варенье. Соц. Хортик. наук. 2005,130, 912-917. [CrossRef]
- 44. МакКаллум, Дж.; Томсон, С.; Питер-Джойс, М.; Кенел, Ф. Анализ генетического разнообразия и разработка маркеров однонуклеотидного полиморфизма в культивируемом луке на основе экспрессируемых маркеров повторения последовательностей. Варенье. Соц. Хортик. наук. 2008,133, 810-818. [CrossRef]
- 45. Болдуин, С.; Питер-Джойс, М.; Райт, К.; Чен, Л.; МакКаллум, Дж. Разработка надежных геномных маркеров повторения простых последовательностей для оценки генетического разнообразия внутри и среди репчатого лука. (Аллиум сера Л.) популяций. Мол. Порода. 2012, 30, 1401-1411. [CrossRef]
- 46. ДеВуди, Дж.А.; Ханикатт, РЛ; Скоу, Л.С. Микросателлитные маркеры у белохвостого оленя. Дж. Херед. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Ходадади, М.; Хасанпана, Д. Иранский лук (Аллиум сера L.) реакция сортов на инбредную депрессию. Мировое приложение. наук. Дж. 2010,11, 426-428.
- 48. Абду, Р.; Бакассо, Ю.; Сааду, М.; Бодуэн, JP; Харди, О.Дж. Генетическое разнообразие нигерийского лука (Аллиум сера L.), оцениваемого с помощью маркеров простых повторов последовательностей (SSR). Акта Хортик. 2016,1143, 77-90. [CrossRef]
- 49. Паван С.; Лотти, К.; Маркотриджано, Арканзас; Маццео, Р.; Бардаро, Н.; Бракуто, В.; Риккарди, Ф.; Таранто, Ф.; Д'Агостино, Н.; Скьявулли, А.; и другие. Особый генетический кластер у культивируемого нута, выявленный путем открытия полногеномных маркеров и генотипирования. Геном растений 2017, 2017,10. [CrossRef]
- 50. Паван С.; Маркотриджано, Арканзас; Чиани, Э.; Маццео, Р.; Зонно, В.; Руджери, В.; Лотти, К.; Риккарди, Л. Генотипирование путем секвенирования дыни (кукумис мело L.) Коллекция зародышевой плазмы из вторичного центра разнообразия выявляет закономерности генетической изменчивости и геномные особенности различных генных пулов. БМС Геном. 2017, 18, 59. [CrossRef]
- 51. Ди Риенцо, В.; Сион, С.; Таранто, Ф.; Д'Агостино, Н.; Монтемурро, К.; Фанелли, В.; Сабетта, В.; Бушеффа, С.; Таменджари, А.; Паскуалон, А.; и другие. Генетический поток среди популяции оливковых деревьев в Средиземноморском бассейне. Пир Дж. 2018, 6. [CrossRef]
- 52. Шеперд, Л.Д.; Маклей, Т.Г. Два микромасштабных протокола выделения ДНК из растительной ткани, богатой полисахаридами. Дж. Плант Рез. 2011,124, 311-314. [CrossRef]
- 53. Дойл, Дж. Дж.; Дойл, Дж. Л. Выделение растительной ДНК из свежей ткани. Фокус 1990,12, 13-14.
- 54. Куль, Дж. К.; Чунг, Ф.; Цяопин Ю.; Мартин, В.; Зевди, Ю.; МакКаллум, Дж.; Катанах, А.; Резерфорд, П.; Раковина, КС; Джендерек, М.; и другие. Уникальный набор из 11,008 XNUMX меток экспрессируемых последовательностей лука выявляет экспрессируемые последовательности и геномные различия между однодольными порядками asparagales и poales. Растительная клетка 2004,16, 114-125. [CrossRef]
- 55. Ким, HJ; Ли, HR; Хён, JY; Песня, К.Х.; Ким, К.Х.; Ким, Дж. Э.; Хур, КГ; Харн, CH. Разработка маркера для тестирования генетической чистоты лука с использованием SSR Finder. Кореец Дж. Брид. наук. 2012, 44, 421-432. [CrossRef]
- 56. Шуэльке, М. Экономический метод флуоресцентного мечения ПЦР-фрагментов. Туземный Biotechnol. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Пикалл, Р.; Смаус, ЧП GenAlEx 6.5: Генетический анализ в Excel. Популяционно-генетическое программное обеспечение для обучения и исследований: обновление. Биоинформатика 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Калиновский, С.Т.; Конус, МЛ; Маршалл, Т.К. Пересмотр того, как компьютерная программа CERVUS учитывает ошибки генотипирования, увеличивает успех в установлении отцовства. Мол. Экол. 2007,16, 1099-1106. [CrossRef]
- 59. Причард, Дж. К.; Стивенс, М.; Розенберг, Н.А.; Доннелли, П. Картирование ассоциаций в структурированных популяциях. Являюсь. Дж. Хам. Жене. 2000, 67, 170-181. [CrossRef]
- 60. Эванно, Г.; Реньаут, С.; Гуде, Дж. Обнаружение количества групп людей с помощью программного обеспечения СТРУКТУРА: моделирование. Мол. Экол. 2005,14, 2611-2620. [CrossRef]
- 61. Эрл, Д.; ФонХолдт, Б. STRUCTURE HARVESTER: веб-сайт и программа для визуализации результатов STRUCTURE и реализации метода Эванно. Консервировать. Жене. Ресурс. 2011, 4. [CrossRef]
- 62. Такезаки, Н.; Ней, М.; Тамура, К. POPTREEW: Веб-версия POPTREE для построения популяционных деревьев на основе данных о частоте аллелей и вычисления некоторых других величин. Мол. Биол. Evol. 2014, 31, 1622-1624. [CrossRef]
- 63. Кумар, С.; Стечер, Г.; Ли, М.; Князь, К.; Тамура, К. МЕГА X. Молекулярно-эволюционно-генетический анализ на различных вычислительных платформах. Мол. Биол. Evol. 2018, 35, 1547-1549. [CrossRef]






























